
正大豐海創(chuàng)新藥FHND1002顆粒納入藥審中心“關愛計劃”試點項目
發(fā)布時間:2024-12-02瀏覽次數(shù):
正大豐海創(chuàng)新藥FHND1002顆粒
納入藥審中心“關愛計劃”試點項目
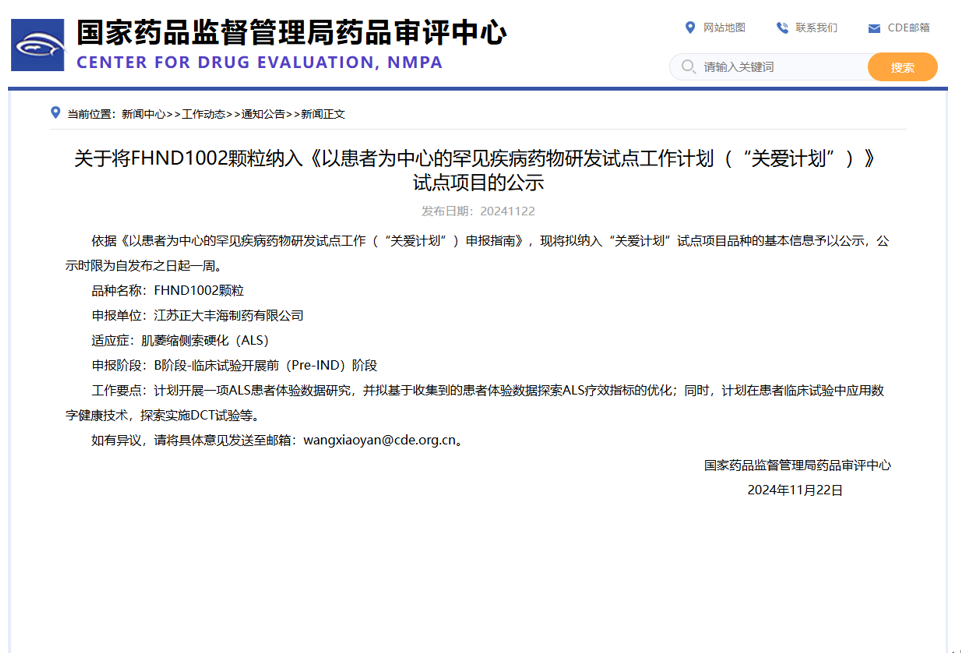
為落實“以患者為中心”的研發(fā)理念,幫助藥企、研究者、監(jiān)管機構(gòu)更好的傾聽罕見病患者需求,以助力藥物研發(fā)的推進和技術要求的優(yōu)化,國家藥品監(jiān)督管理局藥品審評中心啟動以患者為中心的罕見疾病藥物研發(fā)試點工作,即“關愛計劃”(CARE計劃,patient-Centered Action for Rare diseases Encouragement)。
2024年11月22日,藥審中心將正大豐海創(chuàng)新藥FHND1002顆粒納入《以患者為中心的罕見疾病藥物研發(fā)試點工作計劃(“關愛計劃”)》試點項目,正式在藥審中心網(wǎng)站上予以公示,公示無異議的品種最終將被納入“關愛計劃”。
FHND1002顆粒是正大豐海自主研發(fā)的一款First-in-Class(全球首創(chuàng))的小分子藥物,擬用于肌萎縮側(cè)索硬化(漸凍癥)等神經(jīng)退行性疾病,其具有全新的靶點、全新作用機制和全新的化合物結(jié)構(gòu),已于2023年12月獲得肌萎縮側(cè)索硬化適應癥的臨床許可,目前正在中國進行1期臨床試驗。
根據(jù)試點項目納入標準,藥審中心將在五個申報階段中,各選擇1-2個具有代表性的品種納入“關愛計劃”。本次正大豐海FHND1002顆粒入選“關愛計劃”,代表藥審中心對FHND1002作用機制創(chuàng)新性的肯定,更推動正大豐海深入了解罕見病患者需求,繼續(xù)全力推進FHND1002研發(fā)工作。




 蘇公網(wǎng)安備 32098202000163號
蘇公網(wǎng)安備 32098202000163號